国家生物信息中心合作构建“衰老数字人体”
衰老并非由单一基因或通路主导,而是受控于跨越分子到机体的复杂网络。微观扰动在网络中级联放大,驱动宏观衰退与慢病进展。个体差异与器官异步,使同龄人健康储备迥异、老化进程各有快慢。生物技术和人工智能的快速发展,让衰老科学得以突破过去“描述多于预测、关联多于因果”的研究困局,开始尝试回答“一个人有多老”、“哪里先老、为何而老、如何干预”等一系列挑战性问题。
2026年5月8日,国家生物信息中心团队联合中国科学院动物研究所、首都医科大学宣武医院、温州医科大学附属衢州医院、上海交通大学医学院附属仁济医院、南昌大学第一附属医院、同济大学、四川大学华西医院等多家单位,在Cell发表论文“Multimodal clocks of human aging”。研究团队创建了“衰老数字人体”全息框架,将多维度衰老数据映射至个体化数字孪生。在首个概念验证中,团队对覆盖2019名18-91岁健康志愿者的四中心标准化队列(mCAS)进行解析,采集240余项参数,构建了多模态、多层次、可解释的衰老时钟体系,生成可量化、可模拟、可干预的“衰老数字人体”。该框架能精准预测生物学年龄,绘制器官老化异步性图谱,并识别出凝血因子等衰老驱动分子,全面拓展了衰老评估维度。
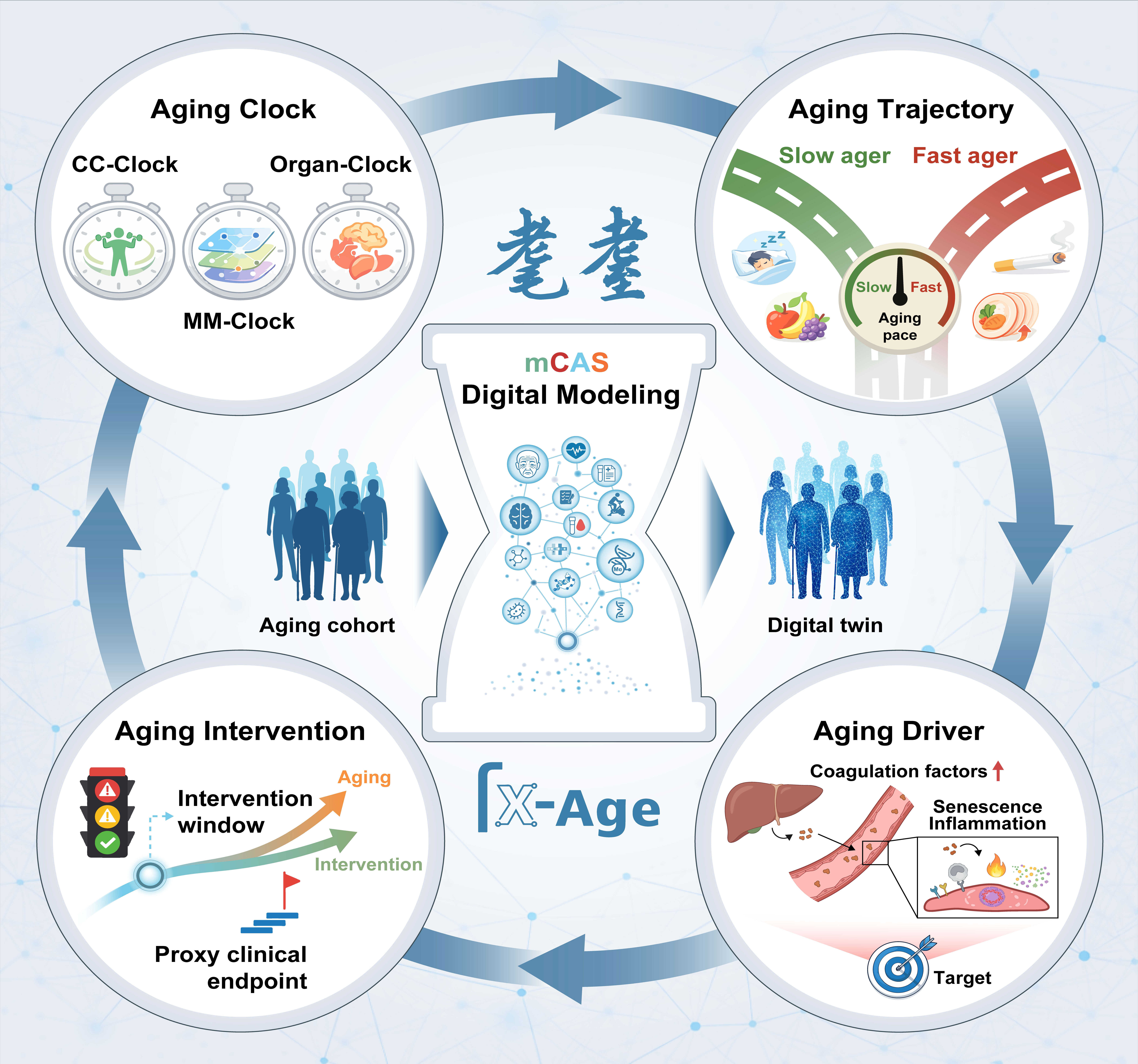
X-Age多维衰老评估与数字建模框架
衰老数字人体的构建遵循“读、算、调”三层逻辑。“读”:获取多维度衰老数据。“算”:利用多模态时钟将数据转化为生物学年龄与器官老化速率。其中,核心能力时钟(CC-clock)整合240余项生理指标;多模态时钟(MM-clock)整合六个层级分子数据,将预测年龄误差降至3.87年;器官时钟依托“液相活检”策略,独立评估六个器官的生物学年龄,揭示衰老异步性。“调”:基于因果推断锁定可靶向的衰老驱动分子。
研究构建了脑、肝脏、肺、肌肉、血管、皮肤六个器官的独立衰老时钟(Organ-clock)。结果显示,器官衰老存在显著异步性,肝脏衰老拐点早于大脑。研究识别出40–50岁和60–70岁两个非线性变化窗口,后者伴随凝血通路显著激活,揭示了衰老加速的关键阶段。
该研究的关键突破在于从相关性走向因果性。团队锁定多个凝血因子的协同上调,明确其来源于衰老肝脏。体外实验证实,关键凝血因子可诱发内皮细胞衰老;小鼠体内实验表明,注射F13B可诱发多组织加速衰老。这些结果证明,特定凝血因子是驱动血管及多器官衰老的核心分子。
临床转化方面,仅用一组代表性血浆蛋白即可近似重建核心时钟,提示血液检测有望成为评估生物学年龄的可行路径。器官特异性衰老时钟可提前识别“超前老化”的器官。衰老数字人体提供差异化干预靶点:对凝血因子驱动的血管老化,可靶向凝血通路;对其他类型,可匹配不同生活方式或药物干预。
该研究标志着衰老科学从描述性向系统性、因果性的范式转变,提出了可量化的生物学年龄作为衰老干预的核心评估指标。
当前,衰老数字人体正持续迭代:引入纵向数据,纳入不同人群,开发低成本检测方案。横断面数据的局限、凝血因子抑制剂尚未完成的验证等问题正被逐步解决。未来,它或成为每个人可及的动态健康孪生引擎,开启标准化、可转化的健康老龄化新路径。