国家生物信息中心联合构建代谢多基因风险评分新模型,精准预测肥胖、糖尿病及其共病风险
肥胖与2型糖尿病是常见的代谢性系统疾病,不仅对个体健康造成长期损害,还会显著增加心血管疾病、肾脏疾病及多种代谢相关并发症的发生风险,已然成为公共卫生领域最主要的挑战之一。国家卫生健康委员会最新发布的监测报告显示,目前我国成人超重率已超过50%。中国疾病预防控制中心慢病中心的一项研究报告表明,2023年我国糖尿病总体患病率已达13.7%,患者总数约为2.33亿,疾病负担持续加重。在临床实践中,肥胖和糖尿病并非孤立发生,而是与多种慢性疾病相互叠加,形成复杂的“多重共病”状态。多重共病不仅加重疾病危害,也显著增加疾病管理的复杂性和医疗保健救治负担。因此,推动慢病防控“关口前移”,在疾病发生之前识别具有较高共病风险的人群,并实施早期干预与精准预防,对于降低慢病及其共病负担具有重要意义。近年来,多基因风险评分(Polygenic Risk Score,PRS)逐渐成为评估复杂疾病遗传易感性的重要工具。PRS通过整合全基因组范围内的遗传风险变异,可以在疾病发生之前识别高风险人群,为早期风险分层和精准医学提供了新的可用工具。PRS在个体出生时即可基于唾液和血液基因组进行计算,是最早量化疾病风险,实现慢病管理关口前移的重要措施。然而,传统PRS通常基于单一疾病或单一表型构建,难以全面反映代谢系统复杂的遗传结构及其多疾病关联特征,因此在疾病预测能力及临床应用潜力方面仍存在一定局限。
近日,国家生物信息中心联合美国博德研究所(Broad Institute of MIT and Harvard)和麻省总院等研究机构,提出了一种新型代谢多基因风险评分模型(Metabolic Polygenic Risk Score,MetPRS),通过整合多种代谢相关性状的遗传关联,该模型能够更准确地预测肥胖和2型糖尿病的发生风险,并进一步识别未来可能发生多种代谢相关并发症的高风险人群,为代谢性疾病的精准风险分层以及多重共病的早期识别与共病管理提供了重要的理论基础和工具支撑。该研究以“Metabolic polygenic risk scores for prediction of obesity, type 2 diabetes, and related morbidities”为题在国际学术期刊 Cell Metabolism 发表。
研究团队系统整合了20种与代谢功能密切相关的性状,包括BMI、腰臀比、腰围、脂肪分布相关指标、糖化血红蛋白、空腹血糖以及胰岛素敏感性等多个代谢维度的表型信息。相关GWAS研究样本累计覆盖超过850万名参与者,为模型构建提供了大规模且多群体的遗传关联数据基础。在此基础上,研究团队分别构建了用于预测肥胖风险的O-MetPRS和用于预测2型糖尿病风险的D-MetPRS,从而实现对两类重要代谢性疾病遗传风险的精准评估。
研究人员首先在英国生物样本库(UK Biobank,N=443,295)队列中开发并验证模型,随后在全球多个独立人群、多遗传背景的研究队列中开展外部验证,包括美国“我们所有人”研究计划(All of Us,N=245,394)、麻省总院生物样本库(Mass General Brigham Biobank,N=53,306),以及沙特阿拉伯研究队列(King Faisal Specialist Hospital & Research Centre,N=6,566)。这些独立验证队列涵盖欧洲、非洲、东亚、南亚、拉丁美洲及中东等多个族裔背景人群,总样本量超过30万人。研究结果显示,MetPRS在不同人群中均表现出稳定且良好的预测性能,并整体优于目前公开数据库中已有的肥胖和糖尿病PRS模型。与现有PRS相比,新模型在肥胖和糖尿病风险预测中的性能分别提升了约30%和20%。并且多队列、多族裔人群的独立验证结果进一步表明,MetPRS在跨人群应用中具有更加稳健的预测能力和更强的泛化性能。在风险分层方面,O-MetPRS识别的最高风险前1%人群中,肥胖患病率达到75.79%;而D-MetPRS识别的最高风险前1%人群中,糖尿病患病率为28.53%。举例而言,2024年我国新生儿数量约为954万,如果将该模型应用于新生儿人群中,仅在出生时即可识别出约9.5万名高遗传风险的个体,其中约7.2万人在未来可能发展为肥胖个体,为疾病的早期预防和精准干预提供了最广阔时间窗口。
研究还系统评估了14种肥胖相关并发症和13种2型糖尿病相关并发症的关联风险。结果显示,MetPRS不仅能够预测肥胖和2型糖尿病本身,还能够识别多种代谢相关并发症的发生风险,整体预测性能优于现有PRS模型。进一步分析发现,在遗传风险评分较高的前20%人群中,O-MetPRS和D-MetPRS分别能够识别出45.9%和44.9%的多病共存高风险个体,表明该模型可以有效筛选出未来更容易同时发生多种代谢相关共病的人群。此外,研究还发现,在约3.7万入组时没有传统风险异常的人群中,遗传得分最高的前10%的个体,在未来超过10年的随访中接受GLP-1受体激动剂治疗的概率增加了约2倍,显示了遗传评分在疾病风险分层与管理中的关口前移作用。将遗传评分纳入到传统危险因素的风险模型中,能够进一步有效提升模型的预测效果,提示遗传因素与传统危险因素的互补作用,整合建模具有更重要的临床应用价值。
该研究由国家生物信息中心、美国博德研究所和麻省总院等机构合作完成。国家生物信息中心汪敏先研究员、美国博德研究所Akl C. Fahed教授以及麻省总医院Patrick T. Ellinor教授为论文的共同通讯作者。美国博德研究所Min Seo Kim博士、国家生物信息中心博士生陈秋丽和美国博德研究所隋阳博士为论文的共同第一作者。本研究得到了中国科学院战略性先导科技专项、国家四大慢病科技重大专项以及国家自然科学基金委员会的资助。
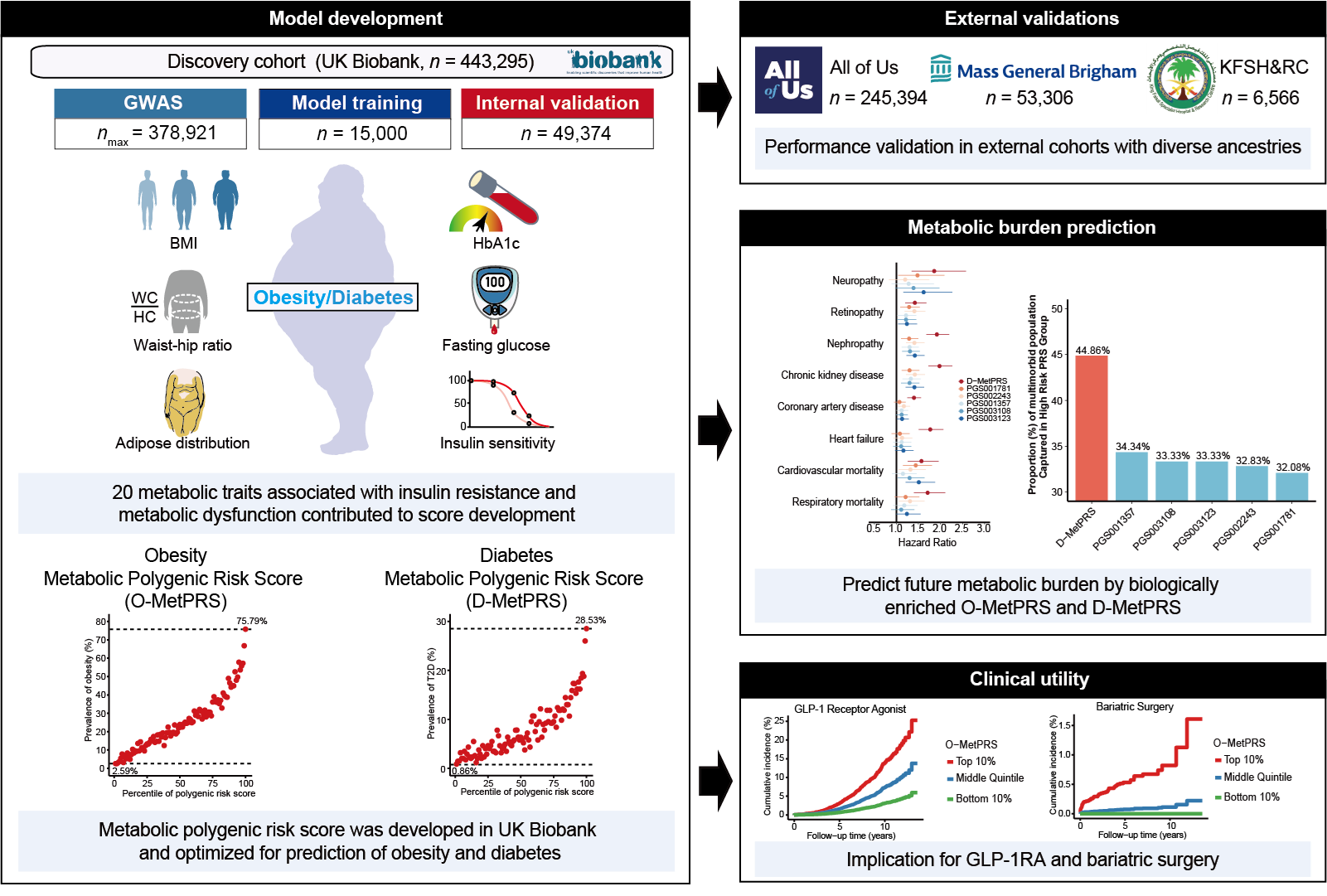
肥胖和2型糖尿病的代谢风险评分模型构建及其临床应用